24.02.26
Федор Иванович ИНОЗЕМЦЕВ
 родился 24 февраля 1802 года в селе Белкино Боровского уезда Калужской губернии
родился 24 февраля 1802 года в селе Белкино Боровского уезда Калужской губернии Результаты конференции по влиянию мобильных устройств и точек раздачи вай-фай на здоровье человека.
Результаты конференции по влиянию мобильных устройств и точек раздачи вай-фай на здоровье человека. 29.01.26
РАК ЖЕЛУДКА - причины болезни
 Этиология рака желудка
Этиология рака желудка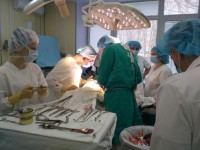 Причинами поздней диагностики рака желудка является:
Причинами поздней диагностики рака желудка является: 30.12.25
ROMA индекс
 НЕ4+СА 125 – комбинация тестов для дифференциальной диагностики злокачественных опухолей и доброкачественных заболеваний яичника
НЕ4+СА 125 – комбинация тестов для дифференциальной диагностики злокачественных опухолей и доброкачественных заболеваний яичника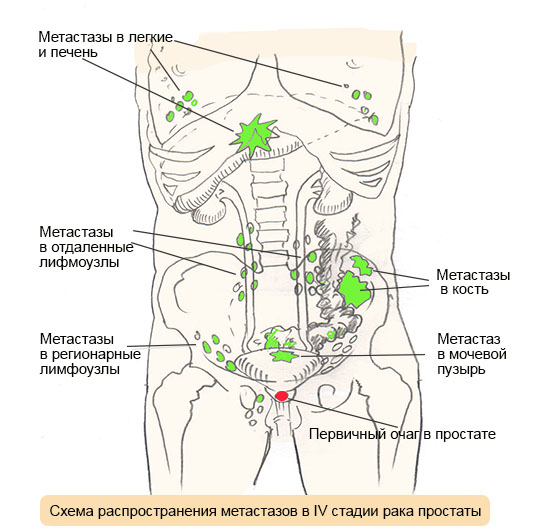 К сожалению, не так редки случаи, когда опухоль, обнаруженная слишком поздно, признается неоперабельной.
К сожалению, не так редки случаи, когда опухоль, обнаруженная слишком поздно, признается неоперабельной.  22 декабря 1939 родился врач-кардиохирург с мировым именем, изобретатель и организатор медицинской науки, педагог, академик – Леонид Антонович Бокерия, более...
22 декабря 1939 родился врач-кардиохирург с мировым именем, изобретатель и организатор медицинской науки, педагог, академик – Леонид Антонович Бокерия, более...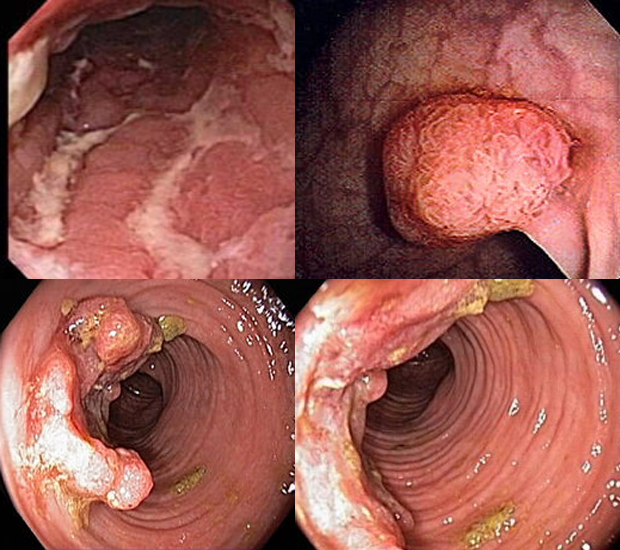 Особое коварство меланомы прямой кишки заключается в её мастерской маскировке под другие менее опасные заболевания. Этим обусловлено, что в 35% при наличии у пациента прямокишечной меланомы допускаются диагностические ошибки.
Особое коварство меланомы прямой кишки заключается в её мастерской маскировке под другие менее опасные заболевания. Этим обусловлено, что в 35% при наличии у пациента прямокишечной меланомы допускаются диагностические ошибки. 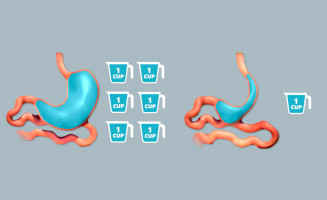 Размер желудка после рукавнной резекции значительно уменьшается, хотя он может варьироваться от пациента к пациенту.
Размер желудка после рукавнной резекции значительно уменьшается, хотя он может варьироваться от пациента к пациенту.
07.12.25
Что такое современная ОНКОХИРУРГИЯ?
 — это баланс между максимальным удалением опухоли и минимальной травмой
— это баланс между максимальным удалением опухоли и минимальной травмой07.12.25
Интимная хирургия для мужчин
 Зачем нужна мужская интимная хирургия?
Зачем нужна мужская интимная хирургия?01.12.25
Психология бариатрической хирургии
 Что будет если сделать человеку бариатрическую операцию и оставить его без послеоперационной поддержки хирурга, терапевта, эндокринолога, психолога?
Что будет если сделать человеку бариатрическую операцию и оставить его без послеоперационной поддержки хирурга, терапевта, эндокринолога, психолога? Ричард Теннант Купер (1885-1957), на его картинах представлены болезни и эпидемии, которыми страдала Англия в различные периоды своей истории.
Ричард Теннант Купер (1885-1957), на его картинах представлены болезни и эпидемии, которыми страдала Англия в различные периоды своей истории. К этим рискам он относит выявляемые при расширенной колоноскопии микрополипы, некоторые из которых (до 1 мм) можно удалять и исследовать непосредственно во время сеанса, визуально и биохимически различимые факторы воспаления кишечной слизистой, изменения в микробиоте, скрытую кровь в верхних отделах толстой кишки
К этим рискам он относит выявляемые при расширенной колоноскопии микрополипы, некоторые из которых (до 1 мм) можно удалять и исследовать непосредственно во время сеанса, визуально и биохимически различимые факторы воспаления кишечной слизистой, изменения в микробиоте, скрытую кровь в верхних отделах толстой кишки Малоинвазивное лечение опухолей мочевого пузыря
Малоинвазивное лечение опухолей мочевого пузыря